
Нині лейкоз великої рогатої худоби (англ. Enzootic bovine leukosis) є одним з найголовніших ворогів молочного та племінного скотарства у багатьох країнах світу. Так, загальнонаціональне опитування в Японії показало високу серопревалентність BLV (Bovine leukemia virus) як у молочної, так і м’ясної худоби (40,9% і 28,7% відповідно). Економічні збитки, завдані цією інфекцією, сягають значних розмірів унаслідок широкого поширення хвороби, зниження продуктивності та якості молочної та м’ясної продукції, передчасного вибракування та забою хворих тварин, ускладнення племінної роботи. На жаль, ця хвороба досі є загрозою для молочного скотарства України.
Збудником лейкозу великої рогатої худоби є РНК-вірус із групи ретровірусів, який має особливий механізм інтеграції свого генетичного матеріалу у геном клітини-господаря, що робить його надзвичайно стійким до дії імунної системи. Заразившись цим вірусом велика рогата худоба пожиттєво залишається інфікованою і з часом у таких тварин розвиваються клінічні ознаки хвороби. Ретровіруси, на відміну від інших вірусів, використовують зворотню транскриптазу (фермент, що каталізує синтез ДНК із використанням РНК як матриці), яка потім «вбудовується» у ДНК клітини господаря. Цей процес інтеграції може призвести до активації онкогенів (особливих генів, що провокують неконтрольований ріст і ділення клітин). Такий складний механізм інтеграції у геном клітини господаря та латентний період після інфікування роблять вірус лейкозу великої рогатої худоби дуже небезпечним, враховуючи неможливість лікування інфікованої худоби. У результаті інфікування цим вірусом у тварин розвивається пухлинне розростання лімфоїдної та кровотворної тканин. Лейкоз ВРХ характеризується тривалим латентним періодом, упродовж якого збудник може не проявляти себе, хоча імунна відповідь організму буде виражатися в утворенні антитіл до нього.
Окремо слід зазначити, що ретровірус, який спричиняє захворювання великої рогатої худоби, не викликає хворобу у людей, однак, м’ясо та молоко від хворих тварин становлять небезпеку для населення і не повинні вживатися в їжу.
Поширення лейкозу є складним безперервним процесом передачі збудника захворювання від заражених до сприйнятливих здорових тварин. Є два шляхи передачі вірусу: вертикальний (внутрішньоутробний) та горизонтальний (контактний). BLV також може передаватися трансплацентарно з інфікованими лімфоцитами матері завдяки здатності останніх мігрувати у міжклітинному просторі і, таким чином, долати плацентарний бар’єр (до 20% телят, отриманих від заражених вірусом BLV корів-матерів, можуть народжуватися вже інфікованими). Крім того, вірус лейкозу може бути присутнім у молозиві та молоці інфікованих корів — випоювання телятам такого молозива або молока індукуватиме у них появу інфекції.
Розповсюдженню лейкозу ВРХ сприяє несвоєчасна діагностика хвороби, недотримання ветеринарних вимог при закупівлі худоби для племінних та виробничих цілей, спільне утримання здорових та інфікованих вірусом лейкозу тварин.
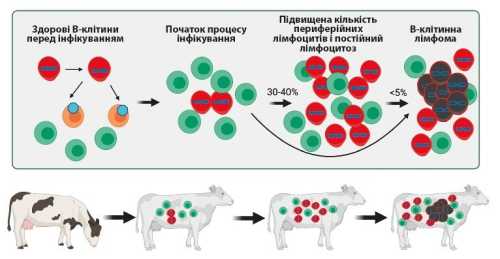
Прижиттєва діагностика лейкозу у ВРХ є обов’язковою!
Прижиттєва діагностика лейкозу ВРХ має вирішальне значення не тільки для визначення ступеня його поширеності, а й для ефективного проведення програми ерадикації лейкозу.
На сучасному етапі в Україні діє державна програма ерадикації лейкозу — серологічній діагностиці (не рідше одного разу на рік) в обов’язковому порядку підлягає все поголів’я великої рогатої худоби, починаючи з 6-місячного віку. При цьому слід зазначити, що дослідження на лейкоз великої рогатої худоби входять до переліку інфекційних хвороб тварин, заходи з профілактики яких та лабораторна діагностика здійснюються за рахунок коштів Державного бюджету (Постанова КМ від 23 квітня 2008 р. № 413). Згідно чинної Інструкції з профілактики та оздоровлення великої рогатої худоби від лейкозу (затверджена наказом Міністерства аграрної політики та продовольства України № 21 від 21.12.2007), основними методами прижиттєвої діагностики лейкозу є серологічні (РІД та ІФА), молекулярно-генетичні (ПЛР) та вірусологічні дослідження, морфологічні аналізи крові та клінічна діагностика хвороби. Наразі основними методами виявлення інфікованих тварин є реакція імунодифузії (РІД) та імуноферментний аналіз (ІФА). І, хоча, РІД та ІФА є серологічними методами діагностики, вони мають значні відмінності з точки зору чутливості та технології виконання.




- Реакцію імунодифузії (РІД) найчастіше використовують для діагностичних досліджень худоби індивідуальних селянських господарств. Це класичний метод, що ґрунтується на преципітації комплексу «антиген-антитіло» в гелі. Він відносно простий у виконанні та доступний за вартістю, проте має певні недоліки — є менш чутливим порівняно з ІФА і може давати хибнопозитивні результати.
- Метод ІФА, зазвичай, застосовують для дослідження поголів’я аграрних підприємств різної форми власності. Це сучасний метод, що також ґрунтується на взаємодії «антиген-антитіло». Виявлення цієї взаємодії відбувається за допомогою антитіл/антигенів із ферментною міткою. Він значно чутливіший, ніж РІД, і дає більш точні результати. Втім, ІФА потребує спеціального обладнання та є дорожчим порівняно з РІД. З іншого боку, всі регіональні державні лабораторії Держпродспоживслужби України мають комплекти обладнання для виконання ІФА-діагностики лейкозу ВРХ. Окрім того, на базі деяких аграрних закладів вищої освіти (зокрема у Білоцерківському НАУ) функціонують науково-дослідні лабораторії, де проводять ІФА та ПЛР-діагностику цієї інфекції на замовлення аграрних підприємств.
- ПЛР використовується при дослідженні особливо цінних тварин або в якості арбітражного методу. Також метод ПЛР є перспективним у разі необхідності дослідження молодняку віком до 6 місяців (обстежувати тварин цієї вікової категорії серологічними методами недоцільно). ПЛР виявляє ДНК провірусу лейкозу у клітинах і є прямим методом діагностики, тому може використовуватися незалежно від стадії імунної відповіді та у разі наявності у теляти колостральних антитіл, а також не дає хибнопозитивного результату.
Тест-набори ІФА: що пропонує сучасний ринок
Актуальним для діагностичних лабораторій є вибір тест-набору ІФА для серологічного дослідження на лейкоз ВРХ. Наразі, на ринку України присутня продукція кількох виробників таких тест наборів, зокрема IDEXX Laboratories (США), INDICAL SVANOVA (Швеція), VMRD (США), INGENASA (Іспанія), ID VET (Франція) — всі вони призначені для серологічного дослідження на лейкоз ВРХ і дозволяють виявити антитіла до збудника інфекції в сироватці крові тварин. Всі згадані тест-системи базуються на принципі зв’язування антигену та антитіла і використовують в якості антигену специфічний білок вірусу лейкозу gp51 (білок gp51 – глікопротеїн, який експресується на поверхні вірусу лейкозу ВРХ). Він є імуногенним, тобто здатний викликати імунну відповідь у тварин, інфікованих вірусом лейкозу, і появу в сироватці крові специфічних до нього антитіл. Тест-системи мають високу чутливість і специфічність (у межах 98–100 %), відносно швидкі у постановці реакції, дозволяють досліджувати велику кількість зразків упродовж відносно короткого періоду часу. Кожна з вищеназваних тест-систем має певні специфічні особливості при постановці реакції, може бути вимоглива до обладнання, має різну тривалість часового діапазону постановки реакції, визначену протоколом виконання дослідження.
Разом із тим, звертає на себе увагу тест-набір «EQUI anti-BLV» від українського виробника ТОВ «Еквітестлаб». Цей ІФА-набір призначений для якісного виявлення сумарних антитіл до вірусу лейкозу великої рогатої худоби у сироватці чи пулі (збірних зразках) сироваток крові, а також у молоці. Особливістю цього набору є те, що він визначає сумарні антитіла до білків gp51 та р24 вірусу лейкозу (білок р24 – структурний білок вірусу, один із основних білків віріону, який є важливою мішенню для імунної відповіді на вірус лейкозу). Поєднання двох імуногенних білків у конструкції тест-набору підвищує його чутливість та специфічність.
«EQUI anti-BLV» базується на принципі «сендвіч-варіанту» твердофазного ІФА в одноетапній інкубації. У лунках планшету засорбовано рекомбінантні антигени gp51 та р24 (аналоги антигенів вірусу лейкозу ВРХ). У кожну лунку додаються зразки сироватки або молока та кон’югант рекомбінантних антигенів з пероксидазою хрону.
У валідаційних дослідженнях із часто використованими в Україні наборами виробництва INGENASA (Іспанія) та ID VET (Франція) (конкурентний імуноферментний аналіз та блокуючий варіант) було показано 100% співпадіння за чутливістю, специфічністю та відсотком співпадіння. Ці комерційні набори, своєю чергою, валідовані референс-лабораторією Міжнародного Епізоотичного Бюро (МЕБ).
У міжфакультетській науково-дослідній лабораторії новітніх методів (ІФА та ПЛР) досліджень Білоцерківського НАУ також були проведені незалежні валідаційні дослідження чутливості та специфічності тест-набіру ІФА «EQUI anti-BLV» у порівнянні з комерційним тест-набором Ingezim BLV Compac 2.0 (INGENASA, Іспанія), який у лабораторії використовується багато років для серологічної діагностики лейкозу ВРХ.
- Метою дослідження було оцінити точність діагностики та зручність використання запропонованого тест-набору вітчизняного виробництва.
- Всього було досліджено 178 зразків сироватки крові, з яких 25 були позитивними і 153 негативними.
- Відповідно до отриманих даних, відносна чутливість тест-системи «EQUI anti-BLV» склала 100%, специфічність – 100%.
- Окрім того, слід відмітити зручність використання набору: упаковка тест-системи компактна, набір укомплектований усіма необхідними для проведення аналізу компонентами.
- Планшет розбірний, що дозволяє відділити необхідну кількість лунок, розміщений у пакеті зі зручною застібкою.
- Реагенти розлиті у ємкості з кришечками різного забарвлення.
- Також забезпечена можливість відстеження внесення реагентів і зразків на кожному етапі аналізу, що значно зменшує вірогідність помилки при виконання аналізу, а процедура виконання дослідження складає всього 2,5 години.
Спираючись на власний досвід використання тест-системи «EQUI anti-BLV» та результати власних порівняльних досліджень можемо з впевненістю рекомендувати цей тест-набір для використання у державних і приватних діагностичних лабораторіях, а також для наукових досліджень.
В. Сахнюк, д-р. вет. наук, професор, член-кореспондент НААН, завідувач науково-дослідною лабораторією молекулярно-генетичних та імунологічних досліджень, Білоцерківський НАУ
Т. Царенко, канд. вет. наук, доцент, завідувач кафедри епізоотології та інфекційних хвороб, Білоцерківський НАУ
Редакційна обробка матеріалу
Л. Крюкова, керівник проєкту «Тваринництво та ветеринарія»
Джерело: propozitsiya.com



